Bộ đề thi vào lớp 10 siêng Hóa năm 2021 gồm đáp án
Với bộ đề thi vào lớp 10 chuyên Hóa năm 2021 bao gồm đáp án được những Thầy/Cô giáo các năm kinh nghiệm tay nghề biên soạn và tổng hợp chọn lọc từ đề thi môn Hóa vào lớp 10 của những trường thpt trên cả nước sẽ giúp học sinh có kế hoạch ôn luyện từ kia đạt điểm cao trong kì thi tuyển sinh vào lớp 10 môn Hóa.
Bạn đang xem: Đề thi vào lớp 10 chuyên hóa

Sở giáo dục và Đào tạo ra .....
Trường thpt ....
Kì thi tuyển sinh vào lớp 10
Năm học 2021
Môn: hóa học (khối chuyên)
Thời gian làm bài: 120 phút
(Đề thi số 1)
Câu 1. (2 điểm)
a/ tại sao CO2 được dùng làm giập tắt đám cháy?
b/ Viết phương trình làm phản ứng và giải thích các hiện tượng kỳ lạ hóa học tập sau:
- vào tự nhiên có tương đối nhiều nguồn tạo nên H2S mà lại lại không có sự tích tụ H2S trong ko khí.
- Trong phòng thí nghiệm, lúc nhiệt kế thủy ngân bị vỡ người ta cần sử dụng bột lưu huỳnh rắc lên sức nóng kế bị vỡ.
- trong phòng thí nghiệm bị độc hại khí Cl2, nhằm khử độc tín đồ ta xịt vào không khí hỗn hợp NH3.
Câu 2. (2 điểm)
1. Cho các thành phần hỗn hợp X bao gồm Al2O3, MgO, Fe, Cu vào hỗn hợp HCl dư thu được dung dịch Y, khí Z và chất rắn A. Tổng hợp A trong dung dịch H2SO4 đặc, nóng, dư nhận được khí B. Sục từ tốn khí B vào hỗn hợp nước vôi vào dư nhận được kết tủa D. Mang lại từ từ hỗn hợp NaOH cho dư vào hỗn hợp Y thì thu được hóa học rắn E. Nung E trong bầu không khí đến cân nặng không đổi thu được hóa học rắn G. Xác định thành phần các chất vào Y, Z, A, B, D, E, G. Biết các phản ứng xảy ra hoàn toàn.
2. Cho tất cả hổn hợp khí bao gồm CO2, C2H4, C2H2, C2H6. Trình bày cách thức hóa học tập để tách bóc riêng từng khí ra khỏi hỗn đúng theo .
Câu 3. (2 điểm)
1. cho các hóa hóa học và vẻ ngoài gồm: can xi cacbua, nước cất, nước brom, ống nghiệm gồm nhánh, ống nghiệm, ống dẫn, nút cao su, ống bé dại giọt, chậu thủy tinh, giá bán đỡ. Trình bày quá trình tiến hành thí nghiệm, nêu hiện tượng, viết phương trình hóa học cho những thí nghiệm sau :
-Điều chế khí axetilen.
-Thu khí axetilen.
-Phản ứng cộng của axetilen.
2.
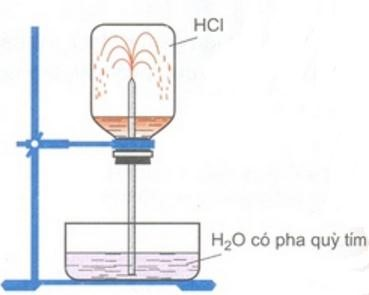
Hình trên minh chứng tính hóa học vật lí gì của khí hiđroclorua? giải thích hiện tượng trên.
Câu 4. (2 điểm)
Hoà tan 34,2 gam lếu láo hợp bao gồm Al2O3 cùng Fe2O3 vào trong 1 lít dung dịch HCl 2M, sau bội nghịch ứng còn dư 25% axit. Mang lại dung dịch sinh sản thành tính năng với dung dịch NaOH 1M làm thế nào để cho vừa đủ đạt kết tủa nhỏ bé nhất.
1.Tính khối lượng của mỗi oxit trong lếu láo hợp.
2.Tính thể tích của hỗn hợp NaOH 1M sẽ dùng.
Câu 5. (2 điểm)
Đốt cháy trọn vẹn chất hữu cơ X (MX 2, H2O cùng N2. Biết số mol H2O bằng 1,75 lần số mol CO2; toàn bô mol CO2 cùng H2O bằng gấp đôi số mol O2 tham gia phản ứng. Xác định công thức phân tử của X.
Đáp án và Thang điểm
Câu 1.
1. A
Khí CO2 nặng rộng không khí và không tác dụng với oxi nên nó có chức năng ngăn quán triệt vật cháy xúc tiếp với ko khí. Cho nên vì thế CO2 được dùng để làm giập tắt các đám cháy.
Tuy nhiên với những đám cháy có sắt kẽm kim loại mạnh (ví dụ: Mg) thì ko được giập lửa bởi CO2 vì chưng sẽ làm các đám cháy trở bắt buộc nghiêm trọng hơn. Do:
2Mg + CO2 2MgO + C
Cacbon hiện ra lại tiếp tục cháy:
C + O2 CO2
1. B
- vào tự nhiên có khá nhiều nguồn tạo nên H2S tuy vậy lại không có sự hội tụ H2S trong ko khí. Vày H2S phản nghịch ứng với O2 trong không gian ở điều kiện thường:
2H2S + O2 → 2S + 2H2O
- Trong chống thí nghiệm, khi nhiệt kế thủy ngân bị vỡ người ta dùng bột lưu hoàng rắc lên nhiệt độ kế bị vỡ. Do Hg cực kỳ độc, lại dễ bay hơi. Trong lúc đó S gồm thể công dụng với Hg ở điều kiện thường tạo ra HgS không phai hơi, góp dễ xử lý hơn.
Hg + S → HgS
- vào phòng nghiên cứu bị ô nhiễm và độc hại khí Cl2, nhằm khử độc tín đồ ta phun vào không khí dung dịch NH3. Do:
2NH3 + 3Cl2 → N2 + 6HCl;
NH3 (k) + HCl (k) → NH4Cl (tt)
Câu 2.
1. Các Phương trình hóa học:
Cho X vào HCl dư:
Al2O3 + 6HCl → 2AlCl3 + 3H2O
MgO + 2HCl → MgCl2 + H2O
Fe + 2HCl → FeCl2 + H2 ↑
Dung dịch Y gồm AlCl3, MgCl2, FeCl2, HCl dư.
Khí Z là H2; chất rắn A là Cu.
Hòa tung A bằng H2SO4 đặc, nóng, dư:
Cu + 2H2SO4 (đặc) CuSO4 + SO2 ↑ + 2H2O
Khí B là SO2. Cho B vào nước vôi vào dư:
SO2 + Ca(OH)2 dư → CaSO3↓ + H2O
Kết tủa D là CaSO3
Cho lỏng lẻo dd NaOH mang lại dư vào Y
NaOH + HCl → NaCl + H2O
3NaOH + AlCl3 → Al(OH)3↓ + 3NaCl
2NaOH + MgCl2 → Mg(OH)2 ↓ + 2NaCl
2NaOH + FeCl2 → Fe(OH)2 ↓ + 2NaCl
NaOH dư + Al(OH)3 → NaAlO2 + 2H2O
Chất rắn E là Mg(OH)2, Fe(OH)2
Nung E ta được G là MgO, Fe2O3.
4Fe(OH)2 + O2 2Fe2O3 + 4H2O
Mg(OH)2 MgO + H2O
2.
- Dẫn hỗn hợp khí qua nước vôi vào dư
CO2 + Ca(OH)2 → CaCO3↓+ H2O
Lọc bóc kết tủa, mang lại phản ứng với HCl thu mang CO2 thoát ra:
CaCO3 + 2HCl → CaCl2 + CO2↑ + H2O
- tất cả hổn hợp khí còn sót lại (C2H4, C2H2, C2H6) dẫn thật chậm rãi qua hỗn hợp AgNO3 / NH3 tất cả dư :
C2H2 +2 AgNO3 + 2NH3 → C2Ag2 ↓ + 2NH4NO3
Hoặc C2H2 + Ag2O
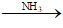
Lọc tách bóc kết tủa rồi cho công dụng với hỗn hợp HCl. Thu khí C2H2 thoát ra:
C2Ag2 + 2HCl → C2H2↑ + 2AgCl ↓
- lếu láo hợp còn lại gồm C2H4 cùng C2H6 cho lội chậm qua dung dịch brom (dư), C2H4 gồm phản ứng, bị duy trì lại. Khí C2H6 ko phản ứng với dung dịch brom thoát ra phía bên ngoài ,thu khí C2H6
C2H4 + Br2 → C2H4Br2
Cho bột Zn (dư) vào trong bình chứa hỗn hợp trên và đun nhẹ, thu khí C2H4
C2H4Br2 + Zn C2H4 ↑ + ZnBr2
Câu 3.
1.
- Điều chế axetilen:
Cho vào ống nghiệm bao gồm nhánh 1 – 2 mẩu can xi cacbua. Đặt ống nghiệm lên giá. Đậy miệng ống nghiệm tất cả nhánh bởi nút cao su đặc có ống nhỏ tuổi giọt. Bé dại từng giọt nước từ bỏ ống nhỏ dại giọt vào ống nghiệm, nước tan xuống xúc tiếp với canxi cacbua, khí axetilen được chế tác thành.
CaC2 + 2H2O → C2H2 ↑ + Ca(OH)2
- Thu axetilen vào ống nghiệm:
Cho đầy nước vào một ống nghiệm, úp ngược ống nghiệm vào chậu đựng nước, luồn đầu ống dẫn vào miệng ống nghiệm cất nước. Axetilen đẩy nước trong ống thử ra, lúc ống nghiệm đầy khí, đem ống nghiệm ra, cần sử dụng nút cao su đậy mồm ống nghiệm lại.
- bội nghịch ứng cùng của axetilen:
Cho đầu chất thủy tinh của ống dẫn khí axetilen sục vào ống thử đựng khoảng tầm 2 ml dung dịch brom, color của dung dịch brom nhạt dần bởi vì axetilen công dụng với brom.
C2H2 + 2Br2 → C2H2Br4
2. thí nghiệm trên chứng tỏ tính dễ dàng tan của hiđroclorua trong nước.
Hiện tượng thí nghiệm: Nước trong chậu theo ống thủy tinh trong phun vào trong bình thành số đông tia nước màu sắc đỏ.
Giải yêu thích hiện tượng:
Khí hiđroclorua tan các trong nước, tạo sự giảm mạnh khỏe áp suất trong bình, áp suất của khí quyển đẩy nước vào cầm chỗ khí HCl sẽ hòa tan.
Dung dịch nhận được là axit buộc phải làm dung dịch quỳ tím gửi sang màu sắc đỏ.
Câu 4.
Gọi x; y theo thứ tự là số mol Al2O3 với Fe2O3 trong hỗn hợp ban đầu.
Theo bài ra: mhh = 34,2 gam → 102x + 160y = 34,2 (1)
Số mol HCl thuở đầu = 2.1 = 2 mol
Số mol HCl dư =
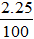
Phương trình hóa học:
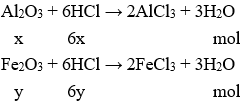
Từ 2 Phương trình chất hóa học suy ra: 6(x + y) = 1,5 (2)
Từ (1) với (2) suy ra x = 0,1 mol ; y = 0,15 mol
a) khối lượng mỗi oxit trong láo lếu hợp:
mAl2O3 = 0,1.102 = 10,2 gam ;
mFe2O3 = 34,2 – 10,2 = 24 gam.
b) dung dịch sau phản nghịch ứng có chứa: AlCl3 0,2 mol; FeCl3 0,3 mol với HCl dư 0,5 mol.
Phương trình hóa học xảy ra:
HCl + NaOH → NaCl + H2O
AlCl3 + 3NaOH → Al(OH)3↓ + 3NaCl
FeCl3 + 3NaOH → Fe(OH)3 ↓ + 3NaCl
Al(OH)3 + NaOH → NaAlO2 + 2H2O
Để cân nặng kết tủa bé bỏng nhất thì Al(OH)3 tan hết trong NaOH, cho nên vì thế kết tủa chỉ tất cả Fe(OH)3
Từ những Phương trình chất hóa học trên suy ra:
Tổng số mol NaOH đề nghị dùng = nHCl dư + 4.nAlCl3 + 3.nFeCl3
= 0,5 + 4. 0,2 + 3.0,3
= 2,2 mol
Vậy thể tích hỗn hợp NaOH đề xuất dùng = 2,2/1 = 2,2 lít.
Câu 5.
Đặt CTPT X là: CxHyOzNt (giả sử: 1 mol)
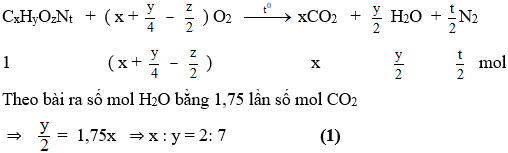
Mặt khác tổng số mol CO2 cùng H2O bằng gấp đôi số mol O2 gia nhập phản ứng:
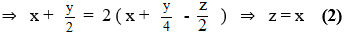
Từ (1) và (2) ⇒ x : y : z = 2:7:2
Công thức phân tử của X có dạng: (C2H7O2Nt)n
Vì MX 2H7O2N
Sở giáo dục và đào tạo và Đào tạo .....
Trường thpt ....
Kì thi tuyển sinh vào lớp 10
Năm học 2021
Môn: chất hóa học (khối chuyên)
Thời gian có tác dụng bài: 120 phút
(Đề thi số 2)
Câu 1. (2,5 điểm)
1. cho các chất: C6H6 (benzen) (l); CH3–CH2–CH3 (k); CH3–C≡CH (k); CH3–CH=CH2 (k); SO2 (k); CO2 (k); FeSO4 (dd); saccarozơ (dd). Hóa học nào có thể làm phai và nhạt màu dung dịch nước brom, lý giải và viết phương trình phản bội ứng hóa học xẩy ra (nếu có).
2. Viết phương trình làm phản ứng hóa học xảy ra (nếu có) khi tiến hành nhiệt phân lần lượt các chất rắn sau: NaNO3; KHCO3; Al(OH)3; (NH4)2SO4.
Câu 2. (2 điểm)
1. Viết công thức cấu trúc và hotline tên của toàn bộ các hóa học ứng với cách làm phân tử C2H4Cl2.
2. Đốt cháy hoàn toàn 3,465gam C2H4Cl2 bởi lượng khí oxi dư, thu được hỗn hợp X (chỉ bao gồm CO2; O2 dư; tương đối nước và khí hiđroclorua). Dẫn trường đoản cú từ toàn bộ lượng X chiếm được vào bình bí mật chứa 925 gam hỗn hợp Ca(OH)2 0,8%, làm phản ứng dứt thu được hỗn hợp Y. Tính cân nặng các hóa học tan gồm trong hỗn hợp Y.
Câu 3. (2 điểm)
Nhỏ thủng thẳng dung dịch chỉ cất chất tan KOH cho đến dư vào thứu tự từng ống nghiệm bao gồm chứa những dung dịch (riêng biệt) sau: HCl (có kết hợp một giọt phenolphtalein); MgCl2; Al(NO3)3; FeCl3; Ca(HCO3)2. Phân tích và lý giải hiện tượng thu được, viết phương trình bội nghịch ứng chất hóa học minh họa.
Câu 4. (3 điểm)
Cho 37,95 gam hỗn hợp bột X (gồm MgCO3 cùng RCO3) vào cốc cất 125,0 gam dung dịch H2SO4 a% (loãng). Khuấy hồ hết hỗn hợp cho tới khi phản bội ứng kết thúc, thu được dung dịch Y; hóa học rắn Z cùng 2,8 lít (ở đktc) khí CO2.
Cô cạn dung dịch Y được 6,0 gam muối khan, còn nung chất rắn Z tới cân nặng không đổi thu được 30,95 gam hóa học rắn T cùng khí CO2.
a. Tính: a (%); trọng lượng (gam) chất rắn Z.
b. Xác định kim một số loại R, biết trong X số mol của RCO3 gấp 1,5 lần số mol MgCO3.
Đáp án và Thang điểm
Câu 1.
1.
+ Benzen: Brom tan trong benzen xuất sắc hơn rã trong nước, khi đến benzen vào nước brom, benzen sẽ phân tách brom tự dung môi nước sang tạo nên nước brom phai và nhạt màu (còn dung dịch benzen – brom màu đã đậm lên).
+ CH3–C≡CH: có phản ứng:
CH3–C≡CH + Br2 → CH3–CBr = CHBr
(Hoặc CH3–C≡CH + 2Br2 → CH3–CBr2–CHBr2)
+ CH3–CH=CH2: gồm phản ứng
CH3–CH=CH2 + Br2 → CH3–CHBr=CH2Br
+ SO2: tất cả phản ứng
SO2 + Br2 + H2O → 2HBr + H2SO4
+ FeSO4: tất cả phản ứng
6FeSO4 + 3Br2 → 2FeBr3 + 2Fe2(SO4)3
+ các chất không làm mất đi màu nước brom: CO2; C3H8 với saccarozơ: vì không tồn tại phản ứng hóa học xảy ra.
Xem thêm: Yoga Giảm Cân Cùng Hồ Ngọc Hà, Hướng Dẫn Các Bài Tập Yoga Hồ Ngọc Hà Đủ 4 Phần
2. các Phương trình hóa học:
2NaNO3 2NaNO2 + O2 ↑(1)
2KHCO3 K2CO3 + CO2 ↑ + H2O (2)
2Al(OH)3 Al2O3 + 3H2O(3)
(NH4)2SO4 2NH3 + H2SO4(4)
Câu 2.
1. những công thức cấu tạo và tên thường gọi tương ứng của chất tất cả CTPT C2H4Cl2 là:
CH3–CHCl2 : 1,1–điclo etan
CH2Cl–CH2Cl: 1,2–điclo etan
2.
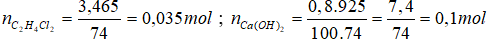
* Phương trình phản bội ứng cháy:
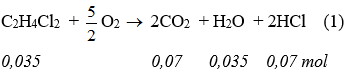
* chưa có người yêu tự xảy ra phản ứng:
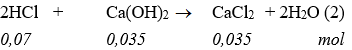
* Số mol Ca(OH)2 sau phản ứng cùng với HCl = 0,1 – 0,035 = 0,065 (mol).
Ta có:
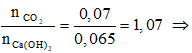
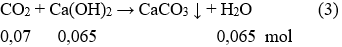
Sau phản bội ứng (3) CO2 dư 0,07 – 0,065 = 0,005 mol
Tiếp tục tất cả phản ứng:
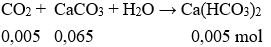
Dung dịch Y gồm các chất tan: CaCl2 0,035 mol với Ca(HCO3)2 0,005 mol
Khối lượng CaCl2 = 0,035. 111 = 3,885(gam);
Khối lượng Ca(HCO3)2 = 0,005.162 = 0,81 (gam)
Câu 3.
* dd HCl có hòa tan một giọt phenolphtalein không có màu. Khi nhỏ KOH vào hỗn hợp này: ban đầu không bao gồm màu (do HCl th-nc KOH bắt đầu cho vào) kế tiếp dung dịch chuyển sang màu hồng (do KOH dư).
Phương trình hóa học:
KOH + HCl → KCl + H2O
* nhỏ KOH đến dư vào dd MgCl2
Hiện tượng: xuất hiện thêm kết tủa trắng ko tan khi KOH dư.
Phương trình hóa học:
2KOH + MgCl2 → Mg(OH)2 (↓ trắng) + 2KCl
* nhỏ KOH mang lại dư vào dd Al(NO3)3:
Hiện tượng: thuở đầu xuất hiện nay kết tủa keo trắng sau đó kết tủa tan khi KOH dư.
Phương trình hóa học:
3KOH + Al(NO3)3 → Al(OH)3 (↓ keo dán giấy trắng) + 3KNO3
KOH dư + Al(OH)3 ↓ → KAlO2 + 2H2O
* bé dại KOH cho dư vào dd FeCl3:
Hiện tượng: xuất hiện kết tủa red color nâu, kết tủa ko tan lúc KOH dư.
Phương trình hóa học:
3KOH + FeCl3 → Fe(OH)3 (↓ đỏ nâu) + 3KCl
* nhỏ tuổi KOH mang lại dư vào dd Ca(HCO3)2:
Hiện tượng: mở ra kết tủa trắng, kết tủa không tan lúc KOH dư.
Phương trình hóa học:
2KOH + Ca(HCO3)2 → CaCO3 (↓ trắng) + K2CO3 + 2H2O
Câu 4.
a/
- mang đến X phản bội ứng cùng với H2SO4 (Thí nghiệm 1)
Số mol CO2 nhận được là:
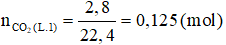
* Nung Z nhận được CO2 → sinh sống thí nghiệm 1 axit H2SO4 thâm nhập pư hết; X dư.
Đặt hỗn hợp X (gồm MgCO3 cùng RCO3) tương tự với muối MCO3.
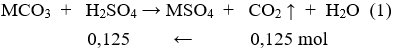
Số mol H2SO4 = số mol CO2 = 0,125 (mol)
Nồng độ % của hỗn hợp H2SO4 là:
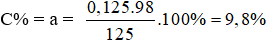
* Số mol cội sunfat SO42- trong muối bột = số mol CO2;
Khối lượng SO42- trong muối bột = 0,125.96 = 12,0 gam > trọng lượng muối rắn khan lúc cô cạn hỗn hợp Y. Vậy trong nhị muối sunfat tạo ra thành có 01 muối bột tan được trong nước (là MgSO4) và 01 muối không tan trong nước (là RSO4).
Vậy dd Y là MgSO4; chất rắn Z là MCO3 dư và RSO4 ko tan.
* Số mol MgSO4 =
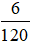
Số mol RSO4 = 0,125 – 0,05 = 0,075mol
* hóa học rắn Z là MCO3 dư và RSO4 không tan; bởi đó:
mZ = 37,95 + 0,075(96 – 60) – 0,05.84 = 36,45(gam).
b/
mZ – mT = mCO2 = 36,45 – 30,95 = 5,5(gam).
Số mol CO2 thu được sau khoản thời gian nung Z =
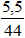
Đặt nMgCO3 = x (mol) ⇒ nRCO3 = 1,5x (mol)
Bảo toàn C: x + 1,5x = (0,125 + 0,125) = 0,25 → x = 0,1 mol
Khối lượng của RCO3 = 37,95 – 0,1.84 = 29,55 (gam)
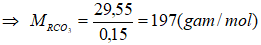
Vậy R là Ba.
Sở giáo dục và đào tạo và Đào sinh sản .....
Trường thpt ....
Kì thi tuyển chọn sinh vào lớp 10
Năm học 2021
Môn: chất hóa học (khối chuyên)
Thời gian làm bài: 120 phút
(Đề thi số 3)
Cho: Ca = 40, Al = 27; fe = 56; C = 12; H = 1; O = 16; cha = 137;
Câu 1. (2,5 điểm)
1. Chỉ được sử dụng một sắt kẽm kim loại duy độc nhất (các dụng cụ quan trọng coi như có đủ), hãy phân biệt các dung dịch đựng trong những lọ mất nhãn sau: K2SO4, Fe(NO3)3, Al(NO3)3, NaCl.
2. Cho một luồng khí H2 (dư) lần lượt đi qua 5 ống mắc thông suốt đựng những oxit được nung lạnh (như hình vẽ):

Hãy xác minh các chất trong từng ống sau thí nghiệm với viết những phương trình chất hóa học xảy ra.
Câu 2. (2,5 điểm)
1. Từ tinh bột và các chất vô cơ bắt buộc thiết, hãy viết các phương trình chất hóa học điều chế: Rượu etylic, polietilen, axit axetic, etyl axetat, metyl clorua, poli (vinyl clorua).
2. Một học viên yêu say đắm môn hóa học, trong chuyến hành trình thăm rượu cồn Thiên Cung (vịnh Hạ Long) có mang lại một chai nước khoáng (nước nhỏ từ nhũ đá trên trần động xuống). Học sinh đó vẫn chia chai nước khoáng làm 3 phần với làm các thí nghiệm sau:
- Phần 1: Đun sôi
- Phần 2: Cho tính năng với hỗn hợp HCl
- Phần 3: Cho tính năng với dung dịch NaOH
Hãy nêu hiện tượng lạ và viết những phương trình hóa học hoàn toàn có thể xảy ra.
Câu 3. (2,5 điểm)
Hỗn phù hợp Z tất cả một hiđrocacbon A với oxi (lượng oxi vào Z gấp rất nhiều lần lượng oxi cần thiết để đốt cháy hết A). Bật tia lửa điện nhằm đốt cháy hỗn hợp Z, đến khi xong xuôi phản ứng thì thể tích khí với hơi sau khoản thời gian đốt không thay đổi so với ban đầu. Nếu mang lại ngưng tụ khá nước của láo lếu hợp sau khi đốt thì thể tích giảm xuống 40% (biết rằng các thể tích khí với hơi những đo nghỉ ngơi cùng điều kiện nhiệt độ cùng áp suất).
1. Xác định phương pháp phân tử của A.
2. Đốt cháy trọn vẹn 8,96 lít khí A (đo ngơi nghỉ đktc) rồi cho cục bộ sản phẩm vào dung dịch đựng 51,3 gam Ba(OH)2 thì khối lượng của dung dịch tăng tốt giảm, bao nhiêu gam?
Câu 4. (2,5 điểm)
Hỗn đúng theo A1 tất cả Al2O3 cùng Fe2O3. Dẫn khí teo qua 21,1 gam A1 cùng nung nóng thu được các thành phần hỗn hợp A2 tất cả 5 hóa học rắn và tất cả hổn hợp khí A3. Dẫn A3 qua dung dịch Ca(OH)2 dư thấy tất cả 5 gam kết tủa. A2 tính năng vừa đủ với một lít hỗn hợp H2SO4 0,5M thu được dung dịch A4 và có 2,24 lít khí thoát ra (đo sinh hoạt đktc).
Tính % trọng lượng mỗi chất trong tất cả hổn hợp A1.
Đáp án & Thang điểm
Câu 1.
1. Chọn sắt kẽm kim loại Ba để dìm biết.
Đánh số thiết bị tự từng lọ mất nhãn, trích mỗi lọ một không nhiều sang ống nghiệm khắc số tương ứng
(trích mẫu thử)
Cho từng mẩu ba vào các mẫu thử:
+ mẫu mã nảo sủi bọt bong bóng khí đồng thời tạo nên kết tủa white là K2SO4.
Phương trình hóa học:
Ba + 2H2O → Ba(OH)2 + H2 ↑
Ba(OH)2 + K2SO4 → BaSO4 (↓ trắng) + 2KOH
+ mẫu mã nào sủi bong bóng khí đồng thời tạo kết tủa nâu đỏ là Fe(NO3)3
Phương trình hóa học:
Ba + 2H2O → Ba(OH)2 + H2 ↑
3Ba(OH)2 + 2Fe(NO3)3 → 2Fe(OH)3 (↓ nâu đỏ) + 3Ba(NO3)2
+ chủng loại nào sủi bọt khí và tạo thành kết tủa trắng keo, tiếp đến kết tủa tan là Al(NO3)3
Ba + 2H2O → Ba(OH)2 + H2 ↑
3Ba(OH)2 + 2Al(NO3)3 → 2Al(OH)3 (↓ trắng keo) + 3Ba(NO3)2
2Al(OH)3 (↓) + Ba(OH)2 → Ba(AlO2)2 + 4H2O
+ mẫu mã nào chỉ sủi bọt khí cùng không thấy gồm kết tủa là NaCl
Phương trình hóa học:
Ba + 2H2O → Ba(OH)2 + H2 ↑
2.
+ Ống 1: không có phản ứng cần sau thí nghiệm vẫn luôn là MgO
+ Ống 2: bao gồm phản ứng:
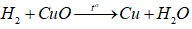
Do H2 dư cần sau thí nghiệm hóa học rắn trong ống 2 là Cu.
+ Ống 3: không có phản ứng buộc phải sau thí nghiệm vẫn luôn là Al2O3.
+ Ống 4: Có những phản ứng:
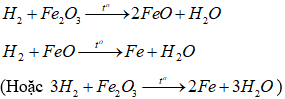
Do H2 dư buộc phải sau thí nghiệm chất rắn trong ống 4 là Fe
+ Ống 5: không có phản ứng nên sau thí nghiệm vẫn luôn là Na2O.
Câu 2.
1. Các phản nghịch ứng chất hóa học điều chế:
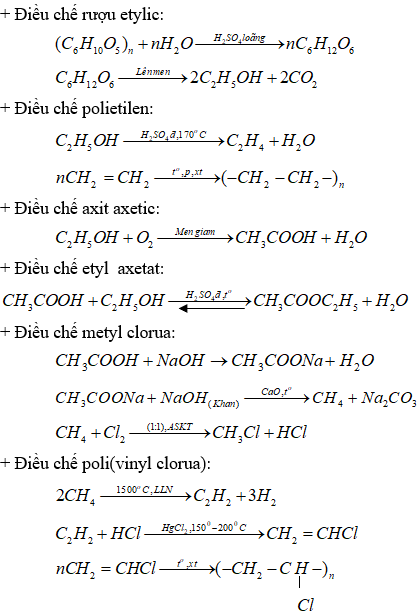
2. Lọ nước bạn làm việc sinh đem lại là hỗn hợp chứa đa số Ca(HCO3)2
+ Phần 1: Đun sôi bao gồm cặn trắng cùng khí xuất hiện do bội phản ứng:
Ca(HCO3)2 CaCO3 + CO2 ↑ + 2H2O
+ Phần 2: Cho tác dụng với dung dịch HCl bao gồm khí bay ra bởi phản ứng:
Ca(HCO3)2 + 2HCl → CaCl2 + CO2 ↑ + 2H2O
+ Phần 3: Cho chức năng với dung dịch NaOH có kết tủa trắng vì chưng phản ứng:
Ca(HCO3)2 + 2NaOH → CaCO3↓ + Na2CO3 + 2H2O
Câu 3.
1. Đặt bí quyết của A là: CxHy (ĐK: x, y nằm trong N*) và thể tích của A lấy đốt là a (lít), (a > 0). Làm phản ứng đốt cháy A.
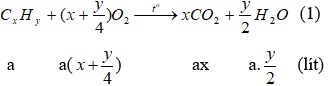
Theo mang thiết lượng oxi đã dùng gấp rất nhiều lần lượng quan trọng và cho khi kết thúc phản ứng thì thể tích khí và hơi sau khi đốt không đổi so với ban đầu nên ta có phương trình:
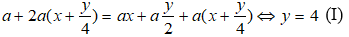
Sau lúc ngưng tụ tương đối nước thì thể tích bớt 40% vị vậy:
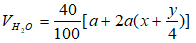
Mặt không giống theo (1) thì
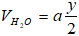
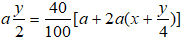
Thay (I) vào (II) ta bao gồm ⇔ x = 1 ⇒ công thức phân tử của A là CH4.
2.
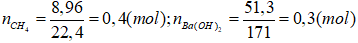
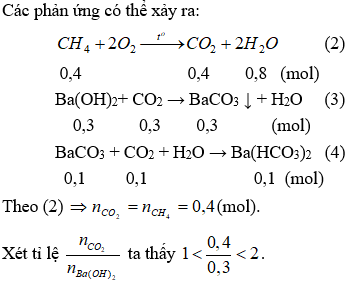
Do vậy xẩy ra cả (3) cùng (4). Lượng BaCO3 sinh ra cực lớn ở (3) kế tiếp hòa tan một trong những phần theo (4).
Theo (3) nBaCO3 = nCO2 = nBa(OH)2 = 0,3 (mol)
Số mol CO2 gia nhập phản ứng ở (4) là: (0,4 - 0,3) = 0,1 (mol).
Theo (4) ⇒ nBaCO3 = nCO2 = 0,1 (mol).
Vậy số mol BaCO3 không trở nên hòa tung sau phản nghịch ứng (4) là: nBaCO3 = 0,3-0,1 = 0,2 (mol).
Ta có: mBaCO3 - mCO2 + mH2O = 0,2.197 - (0,4.44 + 0,8.18) = 7,4 (gam)
Vậy cân nặng dung dịch giảm xuống 7,4 gam.
Câu 4.
Gọi số mol của Al2O3 cùng Fe2O3 trong A1 thứu tự là a và b mol.
Số mol oxi nguyên tử vào A1 là: nO = 3a + 3b mol
Theo giả thiết ta tính được: nH2SO4 = 1.0,5 = 0,5(mol).
Các phản bội ứng hoàn toàn có thể xảy ra:
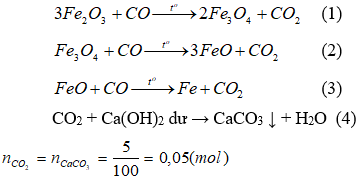
A2 gồm: Al2O3, Fe2O3, Fe3O4, FeO, Fe. Khí A3 là co và CO2;
A2 công dụng với hỗn hợp H2SO4 loãng chiếm được khí chính là khí H2
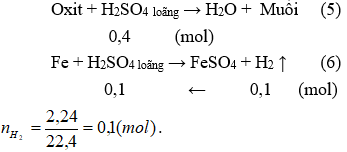
Số mol nguyên tử oxi trong A1 bởi tổng của số mol nguyên tử oxi trong A2 cùng số mol nguyên tử oxi gửi từ teo thành CO2 (hay số mol CO2 ).










